FTAとは? ㈱イーコンプライアンス
FTAとは?
医薬品業界や医療機器業界では、リスクマネジメントにおいて各種のリスクマネジメント手法を持ちいる。
リスクマネジメント手法は著名なものだけでも以下のようなものがある。
- 欠陥モード影響解析(FMEA)
- 欠陥モード影響致命度解析(FMECA)
- 故障の木解析(FTA)
- ハザード分析と重要管理点(HACCP)
- 潜在危険及び作動性の調査(HAZOP)
- 予備危険源分析(PHA)
- リスクランキングとフィルタリング
- 支援統計手法
製造設備のリスクメネジメントにおいては、欠陥モード影響解析(FMEA)が多く用いられる。
一方で、故障の木解析(FTA)は意外とその利用方法が理解されていないことが多い。
FMEAは、「もしこのような故障が発生したら、その結果どのような影響を受けるか」というような質問を体系的に設定する帰納的な手法である。つまりボトムアップ的な手法である。
それに対してFTAは、FMEAとは対称的に、想定した「好ましくない結果」 (危害発生の事故等)から出発する演繹的な方法である。
つまりトップダウン的な手法である。
FTAは、その事象(事故等)をもたらす可能性のある原因や事象を、それ以上分解できない基本事象まで遡って分析する原因解析型手法である。
論理記号(AND、OR等)を用いて図式化することで、複雑な因果関係を把握できるため、想定しにくい事故原因・ハザードの網羅的・早期対策(FMEAの確認・水平展開)や、特定の事故の再発防止対策を講じるための分析手法として有効である。
今、ガスが爆発したという事象(事故)について、FTAを使用して原因分析を試みてみよう。(下図参照)
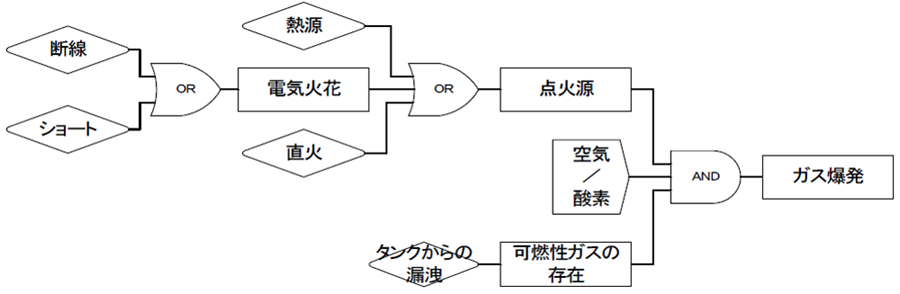
まずガスが爆発するためには、「点火源」と「空気」と「可燃性ガス」が同時に存在しなければならない。
ここで空気をなくすことはできないので「空気」は除外する。
「可燃性ガス」が存在するということは、タンクから漏えいしたこと以外に考えられない。
図においてこの「タンクからの漏えい」はもうこれ以上原因を展開するできないため非展開事象と呼ぶ。
非展開事象はひし形で表す。
次に「点火源」であるが、「熱源」か「電気火花」か「直火」が原因であると考えられる。
「熱源」と「直火」は非展開事象である。
「電気火花」の原因は「断線」または「ショート」である。
「断線」や「ショート」も非展開事象である。
お分かりであろうか。
ガス爆発の再発を防ぐためには、「熱源」や「直火」を遠ざけ、「断線」や「ショート」や「タンクからの漏えい」を防止すれば良いのである。
FTAはこのように事故の原因を究明するのに有効である。
FMEAとFTAを組合せたならば、より確実なリスク分析が実施できる。
一般にFTAは、事故が発生し、その再発防止の目的でCAPAを実行する際などに使用する。
CAPAにおいては「なぜなぜ分析」(5Whys)を実施することがあるが、FTAはそれを上記のように論理記号等を用いてロジカルに根本的原因を究明する。
医療機器の設計変更時などに有効である。
その他、リスクマネジメントに関する詳細は、当社のイーラーニングを参照されたい。
リスクマネジメントに関する書籍
 |
【要点をわかりやすく学ぶ】 製薬・医療機器企業におけるリスクマネジメント |
|
≪ここがポイント≫ 医薬品・医療機器それぞれのリスクマネジメントを初心者にも解りやすく解説! ・リスクマネジメントの全体像の把握と個々のアセスメント手法の理解 ・リスクベースドアプローチとは?? ・FDAが求めるリスク管理と査察対応 ・医薬品・医療機器のリスクマネジメントの差異と各特徴・留意点 ・「リスク」と「ハザード」の違いと各特定方法、マネジメント手法 【発刊日】2015年8月28日 【著 者】株式会社イーコンプライアンス 代表取締役 村山 浩一 |
筆者が常日頃から思ってきたことは、医薬品(ICH-Q9)や医療機器(ISO-14971)に関するリスクマネジメントのセミナーや書籍が皆目ないということである。その理由は定かではないが、おそらくいずれも非常に難解であることと、網羅的に実践した経験者が圧倒的に少ないことに起因するのではないかと思われる。
本書では、医薬品と医療機器のリスクマネジメントを両方取り扱う。医薬品と医療機器では、リスクマネジメントに関する対応方法や対象が異なる。
しかしながらそのプロセスはほぼ同じである。
医薬品と医療機器で、どのようにリスクマネジメントの実施に差異があるかということにも言及した。本書では、難解なリスクマネジメントについて、できる限りわかりやすく執筆したつもりである。本書が、読者諸兄のリスクマネジメントへの理解を深める一助となり、より安全な医薬品・医療機器を世の中に出せることを願っている。
(はじめに 抜粋)
ご購入はこちら。
リスクマネジメントに関する規程・手順書・様式
 |
【ISO14971:2007対応】 リスクマネジメント規程・手順書・様式 |
| ISO14971:2007に沿った形のリスクマネジメント規程・手順書・様式です。 医療機器設計におけるリスク分析は、ISO-14971に従って実施されています。 リスクマネジメント実施のための手順や様式を整えておかなければなりません。 これから作成する医療機器企業やISO-14971認証審査を予定している企業、認証機関から改善指示を受けた企業向けに、サンプルをご用意いたしました。 MS-Word形式ですので、貴社でご自由に加筆・修正を行っていただけます。 |
≪様式一覧≫
※ご注文いただきますと、以下の様式を電子メールにて Wordファイル形式で納品いたします。
・MD-QMS-K5 リスクマネジメント規程
・MD-QMS-S501 リスクマネジメント手順書(ソフトウェアあり)
・MD-QMS-S501 リスクマネジメント手順書(ソフトウェアなし)
・MD-QMS-F501 ハザード項目検討票
・MD-QMS-F502 リスクマネジメントワークシート(ソフトウェアあり)
・MD-QMS-F502 リスクマネジメントワークシート(ソフトウェアなし)
・MD-QMS-F503 リスクマネジメント計画書テンプレート
・MD-QMS-F504 リスクマネジメント報告書テンプレート
ご購入はこちら。


