㈱イーコンプライアンス QMS省令
イーコンプライアンス QMS省令情報
*万が一文中に解釈の間違い等がありましても、当社では責任をとりかねます。
本文書の改訂は予告なく行われることがあります。
QMS省令
QMS省令とは
「医療機器及び体外診断用医薬品の製造管理及び品質管理の基準に関する省令」(QMS省令)
厚生労働省令 第169号
現行のQMS省令は、ISO13485:2003を、一部の用語・内容を薬事法に整合させた形で修正した基準である。
医薬品医療機器等法の施行にあわせて2014年11月25日から施行。
第2章は、ISO13485:2003の各条項と整合した規定とし、第3章(GQP省令に相当)以降は国内における医療機器等の品質等の確保を目的とした追加的要求事項というように区別された。
2018年度内に第2章部分をISO13485:2016に準拠させるための省令改正が行われる予定。
ISO13485:2016に準拠させるべくQMS省令第2章部分を改正予定。
QMS省令第3章部分については第65条が削除になる(第2章の規定と重複するため)こと、体外診断薬不具合報告に関する施行規則条項番号を追加すること以外に基本的に変更なしの予定。
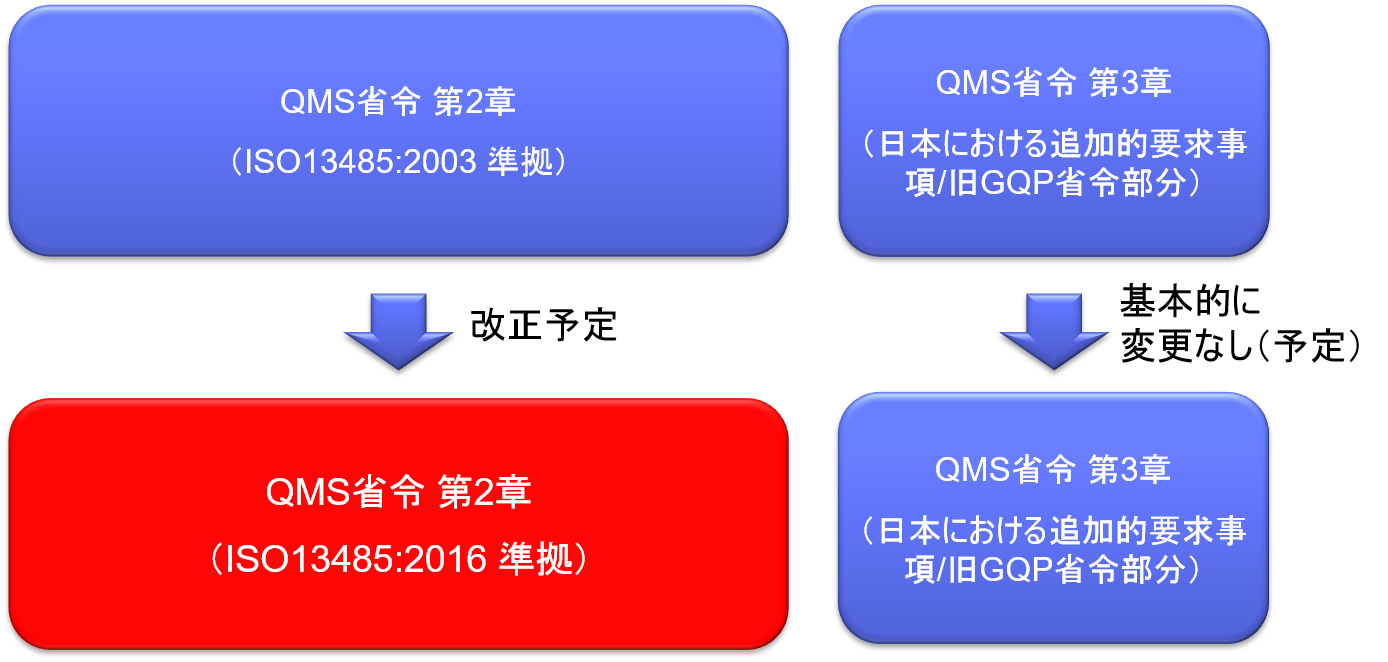
- QMS省令新旧比較
- 「薬事法施行令等の一部を改正する政令(案)等に関する意見の募集の結果について」の考察
- QMS省令医療機器及び体外診断用医薬品の製造管理及び品質管理の基準に関する省令(平成十六年十二月十七日厚生労働省令第百六十九号) 最終改正:平成二六年七月三〇日厚生労働省令第八七号
- QMS省令 逐条解説
- QMS省令逐条解説およびQ&A
- QMS省令作成文書一覧
改正QMS省令(2020年度)
QMS省令の改正
現在のQMS省令第2章部分(ISO13485:2003と同等)をISO13485:2016に準拠させるためにQMS省令を改正
当初では2018年6月にパブリックコメントの実施、10月に新QMS省令の公布・施行が予定されていた。
しかしながら改正手法に関し業界から意見があったため、作業が遅れている。
- 当初は全部改正によりQMS省令を改正する予定であった(省令番号が新規に付与される、条項番号が変わる)。
- 全部改正の場合には省令番号変更による影響が大きいため、業界より一部改正として欲しい旨の要望がなされた。
- 現在一部改正手法による改正とするべく再調整中(省令番号は現行のまま(厚生労働省令第169号)、条項番号は変わらず)。
滅菌バリデーション
(全16講)医療機器QMS規制要件セミナー
【関連記事】
★ 医療機器関連情報
★ 医療機器ソフトウェア関連(IEC-62304、FDA)
★ 製薬関連情報
★ データインテグリティ関連
★ FDA関連情報
★ 品質システム
★ バリデーション
★ J-GMP関連
★ PIC/S関連
★ リスクマネジメント
★ CAPA
★ CSV関連情報
★ Part11関連情報
★ ER/ES指針関連情報
★ EDC関連情報
★ ドキュメント管理システム導入の考え方
用語集








